一、关键信息
发布机构:迈克尔・J・福克斯帕金森病研究基金会(MJFF)联合全球顶尖神经退行性疾病领域专家共同编撰
核心定位:行业最佳实践标准指南,解决 aSyn PFF 模型实验重复性差、病理构建不稳定、操作不规范等行业共性痛点,为帕金森病临床前研究提供标准化、可落地的全流程技术规范。
二、研究背景与行业痛点
1. 帕金森病(PD)研究现状
帕金森病是全球第二大神经退行性疾病,60 岁以上人群发病率约 1%,未来数十年患病率将翻倍增长;
核心病理特征:黑质致密部多巴胺能神经元凋亡、路易小体 / 路易神经突中α- 突触核蛋白(aSyn)异常聚集;
多数散发性 PD 无明确遗传诱因,且疾病具有人类特异性,传统动物模型存在天然局限性,制约发病机制研究与新药研发。
2. 传统 PD 啮齿类模型短板
模型类型 | 优势 | 核心缺陷 |
毒素模型(6-OHDA/MPTP) | 造模快速、运动损伤稳定、时空可控 | 无法模拟 aSyn 路易小体病理;神经元退行性变过快,与人类隐匿发病进程不符,无法用于前驱期治疗筛选 |
基因编辑模型 | 贴合家族性 PD 遗传背景、长期稳定表达致病蛋白 | 缺乏稳定黑质退行性变与可重复运动障碍;表型高度依赖启动子与蛋白表达量,实验重复性差 |
病毒载体模型 | 可同时模拟神经元退变与 aSyn 聚集病理 | 需超生理水平过表达 aSyn,与临床患者生理水平不符;聚集物无纤维结构,无法复刻人类病理特征 |
3. aSyn PFF 模型核心价值与行业难题
模型核心优势
利用重组 aSyn 单体体外组装成预制纤维(PFF),注入啮齿类脑内可触发内源性 aSyn 错误折叠、朊病毒样传播,完美复刻人类 PD 两大核心病理;退行性变进程缓慢,贴合人类从前驱期到运动症状发病的自然病程,生理表达水平更接近临床真实状态,是目前最具转化价值的 PD 临床前研究模型。
行业普遍痛点
各实验室自制 PFF 存在病理诱导不稳定、批次差异大、造模成功率低;缺乏统一制备、验证、给药标准,实验难以重复,浪费研发时间与科研成本。本指南由行业权威制定,统一全流程标准,规避实验坑点。
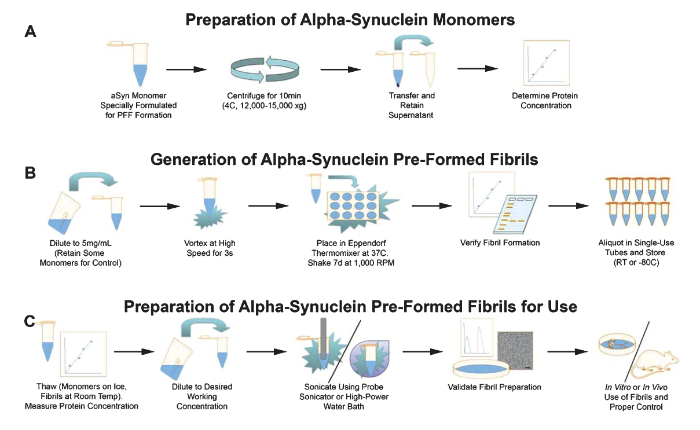
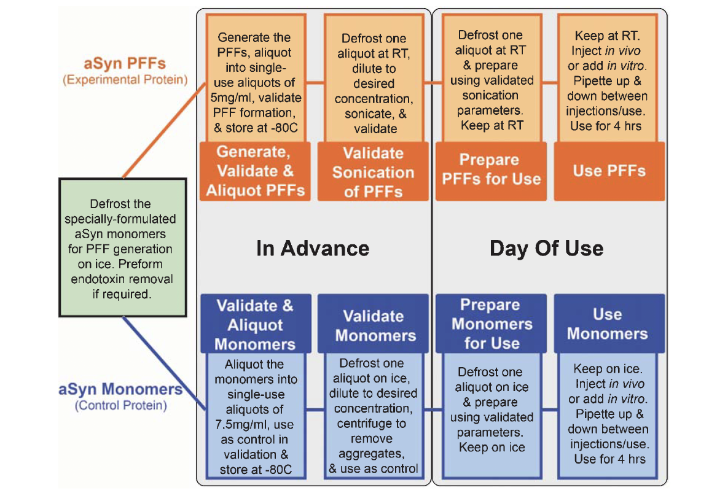
三、aSyn PFF 标准化制备全流程(核心技术要点)
1. 原材料选择
2. 缓冲液与孵育条件标准
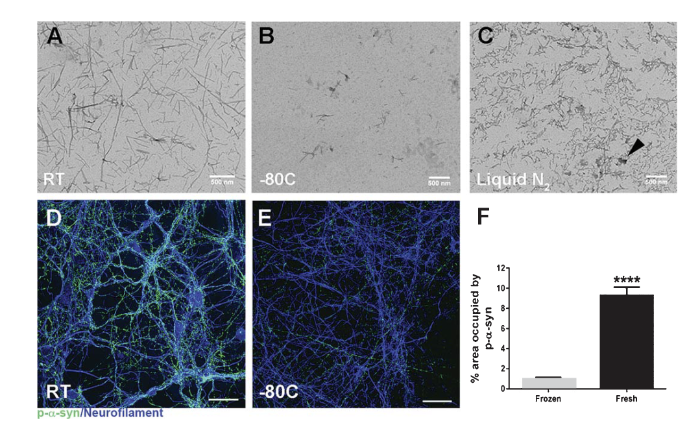
3. 储存与冻融规范(关键避坑点)
单体储存:-80℃分装冻存,全程冰上解冻,避免室温自发聚集;运输需冷链,减少反复冻融。
PFF 成品储存
禁止 4℃/-20℃保存,易发生纤维解离失效;
短期 1–2 周:室温无菌保存;长期 1–1.5 年:-80℃单剂量分装(20–25 μL、5 mg/mL);
严禁液氮速冻,会产生非特异性大聚集体,破坏纤维结构与致病性;
冻存 PFF 使用前必须重新检测蛋白浓度与致病性,冻融会降低病理诱导能力。
4. 超声破碎工艺(决定造模成败)
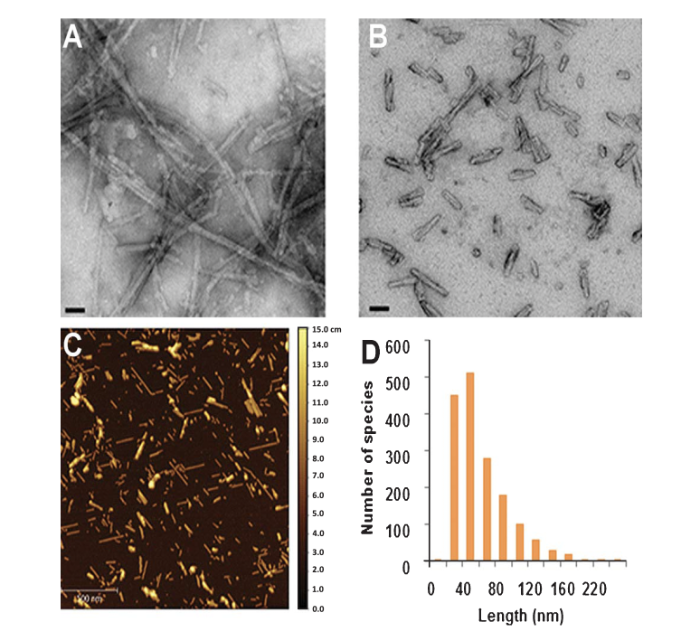
核心要求:超声后纤维长度≤50 nm,是稳定诱导 pS129 aSyn 病理的关键;
超声方式:优先水浴超声(封闭式、控温、无生物气溶胶风险);探针超声需在 BSL-2 生物安全柜操作,15 s 间歇脉冲式超声,控温防热损伤;
适度延长超声时长不破坏纤维淀粉样结构,仅缩小纤维尺寸,提升播种聚集效率;超声后样品室温放置,不可低温冷藏,4 小时内用完。
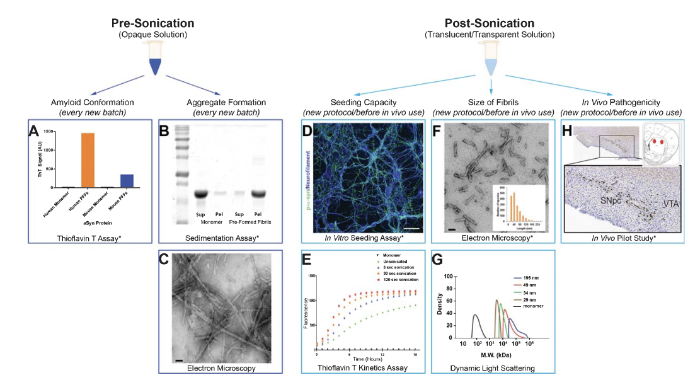
四、PFF 成品质量验证体系(标准化质控)
建立必检 + 补充 + 体内验证三级质控,每批次 PFF 必须完成质控,方可用于细胞 / 动物实验,从源头保障实验可重复性。
1. 纤维形成基础质控(每批次必做)
蛋白浓度检测:Nanodrop A280 直接测定(人 aSyn、鼠 aSyn 采用专属消光系数),或 BCA 法三次稀释重复检测;聚集样品需用盐酸胍解聚后测定。
沉降实验:合格 PFF 绝大部分蛋白沉淀在 pellet 组分,单体则以上清可溶性蛋白为主,判定聚集是否成功。
硫黄素 T(ThT)实验:合格 PFF 荧光信号是单体的 20–100 倍,验证 β- 折叠淀粉样结构形成。
2. 结构与功能补充质控
形貌观测:TEM 透射电镜 / AFM 原子力显微镜,观测纤维长度、形态、纯度,确认超声后粒径≤50 nm;
粒径分析:动态光散射(DLS)快速检测纤维粒径分布,无电镜平台可替代使用;
播种能力检测:原代海马神经元培养、ThT 动力学播种实验,验证 PFF 诱导内源性 aSyn 聚集的活性。
3. 体内预实验验证(长期动物研究必做)
正式长周期造模前,开展 30 天短期啮齿类脑内预注射,检测 pS129 aSyn 病理分布,唯一可直接验证体内致病性的质控手段,避免大规模实验失败。
五、细胞 / 动物实验标准化应用规范
1. 种属匹配原则
PFF 与实验动物种属同源性越高,病理越显著、进展越快:
2. 对照组设置标准(行业首选方案)
3. 体外细胞实验规范
4. 体内脑内注射操作标准
注射靶点:首选背侧纹状体,精准靶向黑质致密部(SNpc),优化坐标可减少 VTA 脑区非特异性病理;
手术参数:注射速率≥0.5 μL/min,注射后留针 2–5 min,避免药液反流;
实验品控:PFF 全程室温放置、每隔吹打混匀;单体对照组全程冰上保存;单日实验样品超声后 4 小时内更换新批次。
适用啮齿类品系:C57Bl/6J、CD-1、SD 大鼠等均适配,可根据病理速度、表型需求选择品系。
六、六大常见实验坑点与标准化解决方案
常见问题 | 解决方案 |
原材料蛋白不兼容,无法形成致病性纤维 | 选用专为 PFF 制备的验证级 aSyn 单体,不使用冻干 / 标签蛋白、不采用旧批次 PFF 留种 |
缓冲液 pH / 离子强度失控,纤维构型异常 | 严格控制 pH≈7.4、NaCl≈100 mM,配制后校准参数再使用 |
储存温度不当,纤维解离失活 | 单体 - 80℃冰上解冻;PFF 仅室温 /-80℃保存,杜绝 4℃/-20℃ |
超声不充分,纤维过长无病理活性 | 标准化超声参数,确保主流纤维粒径≤50 nm,采用水浴 / 间歇探针超声 |
省略质控步骤,盲目开展动物实验 | 严格执行沉降、ThT、电镜、播种实验三级质控,长周期研究必做体内预实验 |
对照组选择不当,实验结果存在干扰 | 优先同批次去内毒素 aSyn 单体为对照,规避蛋白背景、内毒素、自发聚集干扰 |
七、核心总结与商业宣传价值
权威背书:MJFF 牵头 + 全球多所顶尖高校机构专家联合制定,是 aSyn PFF 帕金森病模型国际通用最佳实践指南;
全流程标准化:覆盖原料制备、孵育储存、超声工艺、质控检测、细胞 / 动物实验全链条,统一行业操作规范;
高适配研发场景:适用于帕金森病发病机制研究、神经保护药物筛选、前驱期治疗靶点验证、病理传播机制研究等科研与新药研发领域;
降本增效:规避传统实验批次差异、造模失败、重复性差等痛点,大幅提升实验成功率,节省研发时间与科研投入;
技术落地性强:所有参数、操作流程、质控标准可直接转化为商业化标准化试剂、定制化造模服务、技术外包服务,适配科研院校、药企 CRO 研发需求。
Best Practices for Generating and UsingAlpha-Synuclein Pre-Formed Fibrils to Model Parkinson’s Disease in Rodents
